Le Défi de la Détoxification dans un Monde Chimique
Dans le paysage contemporain de la santé humaine, la fonction hépatique occupe une place centrale, non seulement en tant que régulateur métabolique, mais surtout comme rempart ultime contre une exposition environnementale sans précédent. Depuis l’aube de l’humanité, les traditions médicales, qu’il s’agisse de l’Ayurveda, de la Médecine Traditionnelle Chinoise ou de l’héritage hippocratique, ont accordé une importance primordiale aux processus de « purification » ou de « nettoyage » des humeurs. Autrefois dictée par les rythmes saisonniers et les périodes de disette ou d’abondance, la nécessité de soutenir les émonctoires est aujourd’hui devenue une exigence quotidienne face à l’omniprésence des xénobiotiques (1).
Notre environnement moderne nous soumet à un cocktail complexe de polluants : résidus de pesticides dans l’alimentation, particules fines atmosphériques, métaux lourds, plastifiants (phtalates, bisphénols), médicaments et additifs alimentaires. Cette « charge toxique » ou « body burden » exerce une pression constante sur le foie, l’obligeant à maintenir une activité enzymatique soutenue pour prévenir l’accumulation de substances lipophiles délétères au sein des tissus adipeux et nerveux (1). Lorsque la capacité de traitement du foie est dépassée, ou lorsque les nutriments essentiels aux réactions enzymatiques viennent à manquer, l’homéostasie est rompue, ouvrant la voie à la fatigue chronique, aux troubles métaboliques, à l’inflammation de bas grade et au stress oxydatif systémique.
Cet article propose une analyse exhaustive et rigoureuse des mécanismes physiologiques de la détoxification hépatique et explore comment une approche nutraceutique ciblée, incarnée par la formulation Nutripure Pure Detox, peut offrir une réponse scientifique à ces défis. En s’appuyant sur des données probantes récentes et des extraits végétaux standardisés de haute technicité, nous détaillerons comment soutenir les trois phases de la détoxification pour restaurer la vitalité de l’organisme.
1. Rappel Physiologique Approfondi : Le Foie, Chef d’Orchestre du Métabolisme
Le foie est un organe d’une complexité architecturale et fonctionnelle fascinante. Pesant environ 1,5 kg chez l’adulte moyen, il est stratégiquement positionné pour filtrer le sang provenant du système digestif via la veine porte avant qu’il ne rejoigne la circulation systémique. Cette position de sentinelle lui permet de traiter nutriments et toxines en première ligne.
1.1 Architecture Fonctionnelle et Vascularisation
L’unité fonctionnelle du foie est le lobule hépatique, une structure hexagonale centrée autour d’une veine centro-lobulaire et délimitée par les espaces portes (triades portales) contenant une branche de la veine porte, une branche de l’artère hépatique et un canal biliaire. Le sang s’écoule des espaces portes vers la veine centrale à travers des sinusoïdes, des capillaires fenêtrés qui permettent des échanges intenses avec les hépatocytes. Les hépatocytes, qui constituent 60 à 70 % de la population cellulaire hépatique, sont de véritables usines biochimiques.(1) Ils sont assistés par les cellules de Kupffer (macrophages résidents assurant une surveillance immunitaire) et les cellules stellaires (cellules d’Ito, stockant la vitamine A et responsables de la fibrose en cas d’agression chronique).
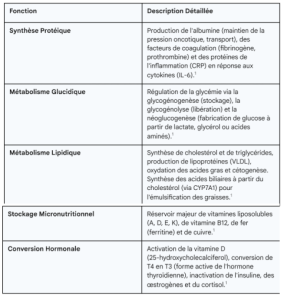
1.2 Les Fonctions Multiples du Foie
Si la détoxification est le sujet central de notre étude, il est crucial de rappeler que le foie assure simultanément plus de 500 fonctions vitales, créant une compétition pour les ressources énergétiques et les cofacteurs nutritionnels.
La fonction de détoxification, ou biotransformation, est énergivore et nutritionnellement coûteuse. Elle nécessite un apport constant en acides aminés, vitamines du groupe B, antioxydants et minéraux. Une carence, même marginale, en l’un de ces cofacteurs peut gripper la machinerie enzymatique.
2. Mécanismes Moléculaires de la Détoxification Hépatique
La détoxification n’est pas un simple filtrage passif, mais une série de réactions enzymatiques séquentielles visant à transformer des molécules hydrophobes (difficiles à éliminer) en dérivés hydrophiles (facilement excrétables dans l’urine ou la bile). Ce processus se déroule en trois phases distinctes mais interdépendantes.
2.1 Phase I : Fonctionnalisation et Bioactivation
La Phase I est la première ligne de défense. Elle se déroule principalement dans le réticulum endoplasmique lisse des hépatocytes et implique la superfamille des enzymes du Cytochrome P450 (CYP450).
- Le Mécanisme Chimique : Les réactions de Phase I (oxydation, réduction, hydrolyse) visent à introduire ou exposer un groupe fonctionnel réactif (comme -OH, -NH2, -SH, ou -COOH) sur la molécule toxique. L’enzyme CYP3A4 est la plus abondante et la plus sollicitée, métabolisant près de 50 % des médicaments et xénobiotiques.
- Le Paradoxe de la Bioactivation : Si cette étape est nécessaire, elle présente un risque majeur. Le métabolite intermédiaire produit est souvent un radical libre ou un électrophile plus réactif et plus toxique que la molécule mère. Par exemple, le paracétamol est transformé en NAPQI, un composé hautement toxique pour le foie s’il n’est pas immédiatement neutralisé.
- Stress Oxydatif Induit : L’activité des cytochromes P450 génère inévitablement des espèces réactives de l’oxygène (ROS). Une induction excessive de la Phase I (par l’alcool, le tabac, certains médicaments, ou des polluants) sans soutien antioxydant adéquat conduit à un stress oxydatif hépatique sévère, endommageant les lipides membranaires, les protéines et l’ADN cellulaire.
2.2 Phase II : Conjugaison et Neutralisation
La Phase II est l’étape de sécurité. Elle consiste à lier le métabolite réactif de la Phase I à une molécule endogène polaire, rendant le complexe hydrosoluble et pharmacologiquement inactif. Cette phase se déroule dans le cytoplasme.
Les principales voies de conjugaison incluent :
- Glucuronidation (UGT) : Utilise l’acide glucuronique. C’est la voie majeure pour l’élimination de la bilirubine, des hormones stéroïdiennes et de nombreux médicaments (morphine, paracétamol).
- Sulfatation (SULT) (1) : Utilise le sulfate (donneur : PAPS) pour conjuguer les stéroïdes, les neurotransmetteurs et certains xénobiotiques phénoliques.
- Conjugaison au Glutathion (GST) : Voie critique pour la neutralisation des électrophiles puissants et la protection contre le stress oxydatif. Les Glutathion S-Transférases (GST) lient le glutathion réduit (GSH) aux toxines.(1) Cette voie est très sollicitée pour les métaux lourds, les solvants et les pesticides.
- Méthylation (MT) : Utilise la S-adénosylméthionine (SAMe) pour méthyler les phénols, les amines et les métaux (comme l’arsenic). (1)
- Acétylation (NAT) : Utilise l’acétyl-CoA pour traiter les amines aromatiques (ex: sulfamides, fumée de cigarette).
L’importance de l’équilibre Phase I / Phase II : Un déséquilibre, caractérisé par une Phase I hyperactive (inducteurs environnementaux) et une Phase II lente (carences nutritionnelles ou polymorphismes génétiques), est pathogène. Il entraîne l’accumulation de métabolites intermédiaires toxiques, favorisant l’inflammation chronique, la carcinogenèse et la sensibilité chimique (1)
2.3 Phase III : Transport et Élimination
Souvent négligée, la Phase III est l’étape finale d’efflux. Elle implique des transporteurs membranaires actifs (famille ABC, comme la P-glycoprotéine ou les MRP) qui pompent les conjugués hydrosolubles hors de la cellule.
- Vers la Bile : Pour les molécules de haut poids moléculaire. Elles seront éliminées via les fèces (nécessité d’un bon transit intestinal pour éviter la réabsorption entérohépatique).
- Vers le Sang : Pour les molécules plus petites, dirigées vers les reins pour une filtration glomérulaire et une élimination urinaire.
3. Une Approche Intégrative : La Synergie Nutripure Pure Detox
Face à la complexité de ces mécanismes, une approche simpliste mono-ingrédient est souvent insuffisante. La formulation Nutripure Pure Detox a été conçue selon une logique de synergie intégrative, visant à moduler harmonieusement les trois phases de la détoxification tout en protégeant l’intégrité de l’hépatocyte. Disponible en deux galéniques (gélules et sachets), elle s’adapte aux besoins spécifiques de l’utilisateur tout en reposant sur un « Core Complex » d’actifs brevetés.
3.1 Le Socle Commun : Une Sélection d’Actifs Brevetés et Objectivés
L’efficacité d’un complément alimentaire repose avant tout sur la qualité et la biodisponibilité de ses ingrédients. Nutripure a sélectionné des extraits labellisés garantissant une standardisation précise en principes actifs.
3.1.1 Le Chardon-Marie (Silactive®) : La Référence en Hépatoprotection
Le Chardon-Marie (Silybum marianum) est utilisé depuis l’Antiquité. Son complexe actif, la silymarine, est un mélange de flavonolignanes (silybine, silychristine, silydianine).(1)
- Le Défi de la Biodisponibilité : La silymarine conventionnelle est très peu soluble dans l’eau et mal absorbée par l’intestin (biodisponibilité de 20 à 50 %).
- L’Innovation Silactive® : L’extrait Silactive® utilisé par Nutripure est un extrait standardisé breveté par Euromed. Des études pharmacocinétiques comparatives démontrent sa supériorité :
- Solubilité accrue : Plus de 75% de l’extrait est dissous après 40 minutes.
- Absorption Maximisée : Les concentrations plasmatiques maximales (Cmax) de silybine sont jusqu’à 30 fois supérieures à celles des extraits standards.
- Excrétion Métabolique : Une récupération urinaire des métabolites 17 fois plus élevée, témoignant d’une utilisation systémique massive.
- Mécanismes d’Action : La silybine agit comme un « bouclier » membranaire, empêchant la pénétration des toxines. Surtout, elle stimule l’ARN polymérase I nucléolaire, accélérant la synthèse des protéines ribosomales et donc la régénération du parenchyme hépatique lésé.1 Elle exerce également une action anti-inflammatoire puissante en inhibant la voie NF-κB et la production de cytokines (TNF-α).
3.1.2 L’Artichaut (Altilix®) : Gestion Métabolique et Cholérèse
L’artichaut (Cynara cardunculus) est bien plus qu’un simple digestif. L’extrait Altilix® (Bionap), issu de cultivars siciliens, est standardisé en acides chlorogéniques (10-12%) et en lutéoline-7-glucoside (2-4%).
- Preuves Cliniques : Une étude randomisée, en double aveugle contre placebo, menée sur 6 mois avec 150 mg/jour d’Altilix®, a montré des résultats remarquables chez des sujets atteints de syndrome métabolique :
- Protection Hépatique : Réduction significative des transaminases (AST, ALT) et de l’Indice de Graisse Hépatique (Fatty Liver Index), indiquant une diminution de la stéatose.
- Optimisation Lipidique : Baisse du cholestérol total, du LDL-cholestérol et des triglycérides.
- Santé Cardiovasculaire : Amélioration de la dilatation médiée par le flux (FMD) et réduction de l’épaisseur intima-média carotidienne.
- Action sur la Phase III : L’extrait d’artichaut est un puissant cholérétique. Il augmente la sécrétion d’acides biliaires (+151% après 1h selon certaines données ), facilitant l’élimination des toxines conjuguées et du cholestérol, tout en stimulant le péristaltisme intestinal pour prévenir la réabsorption des déchets.
3.1.3 Le Chou Kale (PureBlackKale®) : L’Activation Épigénétique Nrf2
L’intégration du Chou Kale noir (Brassica oleracea var. viridis), sous la forme de l’extrait PureBlackKale®, marque le caractère avant-gardiste de la formule.
- La Voie du Sulforaphane : Cet extrait est titré en glucosinolates, et spécifiquement en glucoraphanine. Une fois ingérée et hydrolysée (par la myrosinase végétale ou le microbiote intestinal), la glucoraphanine libère du sulforaphane.
- Le « Maître Interrupteur » Nrf2 : Le sulforaphane est l’un des activateurs naturels les plus puissants du facteur de transcription Nrf2. En condition basale, Nrf2 est séquestré dans le cytoplasme par la protéine Keap1. Le sulforaphane modifie la conformation de Keap1, libérant Nrf2 qui migre vers le noyau.
- Réponse Antioxydante Massive : Dans le noyau, Nrf2 se lie aux séquences ARE (Antioxidant Response Element) de l’ADN, déclenchant la transcription simultanée de dizaines de gènes de cytoprotection :
- Enzymes de Phase II : Glutathion S-Transférases (GST), Quinone Réductase (NQO1), UDP-glucuronosyltransférases (UGT).
- Antioxydants endogènes : Superoxyde Dismutase (SOD), Catalase, Hème Oxygénase-1 (HO-1).
- Synthèse du Glutathion : Gamma-glutamylcystéine ligase. C’est une stratégie de « stimulation des défenses endogènes » bien plus puissante que l’apport passif d’antioxydants.
3.1.4 Les Cofacteurs Indispensables : NAC et Choline
Pour fonctionner, ces enzymes ont besoin de carburant.
- N-Acétyl-Cystéine (NAC) : Elle apporte la L-Cystéine, l’acide aminé limitant pour la synthèse du Glutathion.(1) Sans cystéine suffisante, la production de glutathion s’effondre, laissant le foie vulnérable au stress oxydatif de la Phase I.
- Choline (VitaCholine®) : La Choline bitartrate (sous forme d’acide tartrique L(+) naturel) est essentielle à la synthèse de la phosphatidylcholine, un constituant majeur des membranes cellulaires et des VLDL (Very Low Density Lipoproteins).(1) Les VLDL sont nécessaires pour exporter les triglycérides hors du foie. Un déficit en choline favorise la stéatose hépatique (foie gras) et la mort cellulaire.(1)
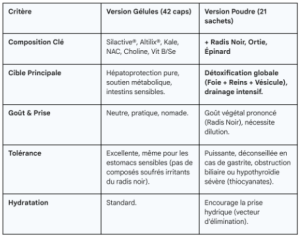
4. Gélules ou Sachets : Quelle Galénique pour Quel Besoin?
Si le « Core Complex » (Silactive + Altilix + Kale + NAC + Choline + Vitamines) est présent dans les deux versions, la forme Poudre (Sachets) bénéficie d’une matrice végétale enrichie qui en fait un outil de drainage plus global.
4.1 La Version Poudre : La Synergie « Drainage Total »
La version sachet intègre trois ingrédients supplémentaires qui ciblent les émonctoires secondaires et renforcent l’action hépatique : le Radis Noir, l’Ortie et l’Épinard.(15)
4.1.1 Le Radis Noir (Raphanus sativus var. niger)
Pilier de la phytothérapie traditionnelle, le Radis Noir est ici justifié par des mécanismes moléculaires précis.
- Induction Enzymatique Biphasique : Riche en glucosinolates (glucoraphasatine), le radis noir induit significativement les enzymes de Phase I (CYP1A1, CYP1A2) et de Phase II (Quinone Réductase, GST, HO-1).(17) Des études in vivo montrent qu’il accélère la clairance des toxines du sang.
- Drainage Mécanique : Il exerce une action cholagogue puissante, favorisant la contraction de la vésicule biliaire et l’évacuation de la bile, « débouchant » ainsi les voies d’élimination hépatiques souvent encombrées.
- Protection et Régénération : Des études sur rats intoxiqués au tétrachlorure de carbone (CCl4) montrent que l’extrait de radis noir fermenté réduit la peroxydation lipidique et les niveaux d’ALT/AST, témoignant d’un effet hépatoprotecteur comparable à la silymarine.(21)
4.1.2 L’Ortie (Urtica dioica) : L’Axe Reins-Foie
L’Ortie est incluse pour son action sur l’émonctoire rénal et son soutien métabolique.
- Élimination Rénale (Phase III urinaire) : L’ortie possède des propriétés diurétiques et natriurétiques reconnues, facilitant l’excrétion urinaire des xénobiotiques hydrosolubles produits par la Phase II hépatique. (23) Elle aide également à l’élimination de l’acide urique et de l’urée.
- Hépatoprotection Antioxydante : L’extrait d’ortie restaure les niveaux de glutathion réduit et de catalase dans le foie face à un stress toxique, protégeant les membranes hépatocytaires de la peroxydation. Elle module également l’activité des cytochromes, limitant potentiellement l’emballement de la Phase I.
- Reminéralisation : Riche en silice et minéraux, elle compense les pertes potentielles liées à la diurèse et soutient la vitalité globale (effet adaptogène léger).
4.1.3 L’Épinard (Spinacia oleracea) : Densité Nutritionnelle
La poudre d’épinard apporte une matrice riche en polyphénols, chlorophylle et bétaïne.
- Protection contre la Lipotoxicité : Des recherches indiquent que les antioxydants de l’épinard protègent l’ADN leucocytaire des dommages oxydatifs et réduisent l’accumulation de lipides hépatiques induite par des régimes hypercaloriques.
- Soutien mitochondrial : Les extraits d’épinard semblent améliorer l’efficacité mitochondriale, cruciale pour fournir l’ATP nécessaire aux réactions de détoxification.
4.2 Tableau Comparatif : Choisir sa Cure
5. Stratégie Chronobiologique et Recommandations
Nutripure intègre une dimension souvent oubliée : la chronobiologie hépatique.
5.1 Pourquoi une Prise Nocturne?
Le foie est soumis à un rythme circadien strict, régulé par des gènes « horloge » (Clock, Bmal1).
- Phase Diurne (Jour) : Le foie est orienté vers la production d’énergie, la synthèse de glycogène, la production de bile et la synthèse protéique pour soutenir l’activité physique et la digestion.1
- Phase Nocturne (Nuit) : C’est la phase de « maintenance ». Le foie bascule vers la détoxification des xénobiotiques, la régénération cellulaire (mitose des hépatocytes) et la réparation de l’ADN endommagé.1 Selon la Médecine Traditionnelle Chinoise, l’énergie du foie est maximale entre 1h et 3h du matin.
- La Stratégie Nutripure : En recommandant la prise du produit (2 gélules ou 1 sachet) le soir, on fournit les substrats et les inducteurs juste avant cette fenêtre d’opportunité métabolique. Cela maximise la biodisponibilité des actifs au moment précis où les enzymes de détoxification et de réparation sont les plus actives.
5.2 Protocoles de Cure
- La Cure de Saison (Printemps/Automne) : Utiliser la version Sachet pendant 21 jours. Cette durée correspond à un cycle biologique permettant une régénération cellulaire significative sans épuiser l’organisme. Le drainage global (foie/reins) est idéal pour les transitions saisonnières.
- Le Soutien Continu ou Ciblé : Pour les sportifs en période de charge, les personnes sous traitement chronique (avec accord médical) ou celles ayant une digestion difficile des graisses, la version Gélules peut être utilisée en cures régulières ou en entretien, offrant une protection hépatique sans l’effet purgatif du radis noir.
- Synergie Alimentaire : La cure doit s’accompagner d’une réduction des toxiques (alcool, tabac, aliments ultra-transformés) et d’une hydratation abondante (min. 2L d’eau/jour) pour soutenir le travail rénal sollicité par l’ortie et la mobilisation des toxines.
Conclusion
La détoxification hépatique n’est pas un concept marketing vague, mais une réalité physiologique complexe qui conditionne notre vitalité, notre immunité et notre équilibre métabolique. Dans un environnement de plus en plus toxique, soutenir cette fonction n’est plus une option, mais une nécessité de santé publique.
La formulation Nutripure Pure Detox s’impose comme une référence dans le domaine de la nutraceutique fonctionnelle. En refusant les compromis sur la qualité (extraits brevetés Silactive® et Altilix® à haute biodisponibilité) et en intégrant les dernières avancées sur la voie Nrf2 (PureBlackKale®), elle offre une réponse scientifique aux mécanismes de Phase I, II et III.
L’approche duale — Gélules pour l’hépatoprotection et la tolérance, Sachets pour le drainage émonctoriel global — permet au praticien de santé naturelle et à l’utilisateur averti de personnaliser la stratégie de détoxification. En respectant la chronobiologie et en fournissant les cofacteurs essentiels (NAC, Choline), Nutripure Pure Detox ne se contente pas de drainer ; il protège et régénère le foie, véritable gardien de notre santé globale.
Envie d’en savoir plus sur Nutripure ou de recommander nos produits ? Écrivez-nous à prescription@nutripure.fr ou consultez notre page dédiée juste ici
Références bibliographiques
(1) Mice with humanized livers reveal the role of hepatocyte clocks in rhythmic behavior /Anne Sophie Delbès et al, science advances 17 may 2023
(2) The liver by day and night 1Rona Aviram et al, The journal of hepatology volume 74, Issue 5 pages 1240 -1242
(3) The role of circadian timing system on drug metabolism and detoxification Fre´de´ric Gachon et Al expert opinion 2011 147-158
(4) Ceccarelli, N. et al. The role of Cynara scolymus in traditional and modern medicine. Ethnobotany Research and Applications, 2010.
(5) Lattanzio V, Paul AK, Lansalta V, Cardinali A (2009) Globe artichoke: a functional food and source of nutraceutical ingredients. J Funct Foods 1:131–144
(6) Agricultural Research service , Dr DUke’s phytochemical and ethnobotanist databases
(7) Bruneton J pharmacognosy, phytochemistry, medicinal plants (paris lavoisier 193 218-219 Blumenthal M Herbal medicine Expanded commission and monographs 2000 10-12
(8) T. Adzet 1,Hepatoprotective activity of Cynara scolymus polyphenolic compounds against CCl4 toxicity in isolated rat hepatocytesMeta-Analysis
(9) Mehmetçik G, Ozdemirler G, Koçak-Toker N, Cevikbaş U, Uysal M. Effect of pretreatment with artichoke extract on carbon tetrachloride-induced liver injury and oxidative stress. Exp Toxicol Pathol. 2008 Sep;60(6):475-80. doi: 10.1016/j.etp.2008.04.014. Epub 2008 Jun 25. PMID: 18583118.
(10) Gebhardt, R. et Fausel, M. Pharmacological effects of artichoke extract on the bile flow and lipid levels in the liver. Journal of Phytotherapy, 1997. Cette étude a confirmé les propriétés cholérétiques de la cynarine
(11) Salem, MB, Affes, H., Ksouda, K. et al. Études pharmacologiques de l’extrait de feuille d’artichaut et de ses bienfaits pour la santé.
(12) Plant Foods Hum Nutr 70 , 441–453 (2015). https://doi.org/10.1007/s11130-015-0503-8.
(13) Kraft K (1997) Artichoke leaf extract–recent findings reflecting effects on lipid metabolism, liver, and gastrointestinal tracts. Phytomedicine 43:69–78
(14) Matuschowski JP (1996) Testing of Cynara scolymus in the isolated perfused rat liver. 43rd Ann Congr Soc Med Plant Res 10:103–107
(15) Kirchhoff R, Beckers C, Kirchhoff GM, Trinczek-Gärtner H, Petrowicz O, Reimann HJ. Increase in choleresis by means of artichoke extract. Phytomedicine. 1994 Sep;1(2):107-15
(16) Salekzamani S., Ebrahimi-Mameghani M., Rezazadeh K. The antioxidant activity of artichoke (Cynara scolymus): A systematic review and meta-analysis of animal studies. Phytotherapy Research. 2018;1–17.
(17) Metabolic and Anti-Inflammatory Protective Properties of Human Enriched Serum Following Artichoke Leaf Extract Absorption: Results from an Innovative Ex Vivo Clinical Trial Fabien Wauquier et al, 10 june 2021 Nutriments 2021
(18) Skarpanska-Stejnborn, Anna et al. “The influence of supplementation with artichoke (Cynara scolymus L.) extract on selected redox parameters in rowers.” International Journal of Sport Nutrition and Exercise Metabolism 18,3 (2008): 313-27. doi:10.1123/ijsnem.18.3.313
(19) Nutrients. 2019 Oct 25;11(11):2580. doi: 10.3390/nu11112580.Altilix® Supplement Containing Chlorogenic Acid and Luteolin Improved Hepatic and Cardiometabolic Parameters in Subjects with Metabolic Syndrome: A 6 Month Randomized, Double-Blind, Placebo-Controlled Study
(20) Morazzoni, P et al Silybum marianum (µCardus marianus), Fitoterapia. 1995, 66:3-42
(21) Foster S Milk thistle 1st edition 5Austin TX american Botanical council 1990
(22) Hobbs c Milk Thistle The liver herb , second edition (Capiitola, Botanica Press, 1994
(23) Comparative study of flavonolignan pharmacokinetics after consumption of a conventional milk thistle extract vs SILACTIVE in healthy volunteers. »
(24) Bruneton J pharmacognosy, phytochemistry, medicinal plants (paris lavoisier 193 249-251
(25) Blumenthal M Herbal medicine Expanded commission and monographs 2000 257-263
(26) Wu JPet Al, Sylimarin accelerates liver regeneration after partial hepatectomy .eviendetbase Complement, Alter medecin 2015 603529
(27) Nature sciences santé édition 21 decembre 2019
(28) Silybin, a component of sylimarin, exerts anti-inflammatory and anti-fibrogenic effects on human hepatic stellate cells Marco trappoliere et Al, journal of hepatology, june 2009
(29) Valenzuela A, Aspillaga M, Vial S, et al: Selectivity of silymarin on the increase of the glutathione content in different tissues of the rat. Planta Med 55(5):420-422, 1989. doi: 10.1055/s-2006-962056
(30) Bahari H, Shahraki Jazinaki M, Rashidmayvan M, Taheri S, Amini MR, Malekahmadi M. The effects of silymarin consumption on inflammation and oxidative stress in adults: a systematic review and meta-analysis. Inflammopharmacology. 2024;32(1):949-963
(31) Ward J, Kapadia K, Brush E, et al: Amatoxin poisoning: case reports and review of current therapies. J Emerg Med 44(1):116-121, 2013. doi: 10.1016/j.jemermed.2012.02.020
(32) Pellegrini L, Belcaro G, Dugall M, Hu S, Gizzi G, Corsi M, Hosoi M, Luzzi R, Feragalli B, Cotellese R. Supplementary management of functional, hepatic damage with Liverubin (pharma-standard Silymarin). A 3-month registry. Minerva Gastroenterol Dietol. 2015 Oct 8.
(33) Predominant aliphatic glucosinolates in kale are reported to be sinigrin, glucoiberin and glucoraphanin (Charron, Saxton and Sams 2005; Velasco et al., 2007; Sasaki et al., 2012; Korus, Słupski, Gebczynski and Bana 2014)
(34) Kapusta-Duch, J., et al. (2012). Beneficial effects of Brassica genus vegetables on human health. Rocz Panstw Zakl Hig (Annals of the National Institute of Hygiene), 63(1), 34-41.
(35) The beneficial effects of Brassica vegetables on human healthJoanna Kapusta-Duch 1, Aneta Kopeć, Ewa Piatkowska, Barbara Borczak, Teresa Leszczyńska Rocz Panstw Zakl Hig 2012;63(4):389-95.
(36) Epub 2018 24 avril.Le chou frisé ( Brassica oleracea var. acephala ) comme superaliment : examen des preuves scientifiques à l’origine de cette affirmation Dunja Šamec 1, Branimir Urlić 2, Branka Salopek-Sondi 1
(37) Front. Pharmacol., 29 August 2023 Sec. Gastrointestinal and Hepatic Pharmacology Volume 14 – 2023 | https://doi.org/10.3389/fphar.2023.1256029 Therapeutic potential of sulforaphane in liver diseases: a review
(38) Efficacy of a Supplement Containing Broccoli Sprout Extract on Liver Function in Healthy Adults – A multicenter, randomized, double-blind, placebo-controlled, parallel-group study. Japanese Pharmacology and Therapeutics (Jpn Pharmacol Ther), Vol. 46, No. 1, 2018, pp. 81-108. Masahiro Kikuchi, Yudai Aoki, Koichi Aizawa, Hiroyuki Suganuma, Yasuhiro Nishizaki. Tokai University Tokyo Hospital et Kagome Corporation Innovation Headquarters. 2018.
(39) Marzullo L. An update of N-acetylcysteine treatment for acute acetaminophen toxicity in children. Curr Opin Pediatr. 2005;17(2):239‐245. doi:10.1097/01.mop.0000152622.05168.9e